La vacuna de Moderna muestra una eficacia del 94,5% en el primer análisis del ensayo fase 3
La compañía solicitará una autorización de uso de emergencia en Estados Unidos en "las próximas semanas"
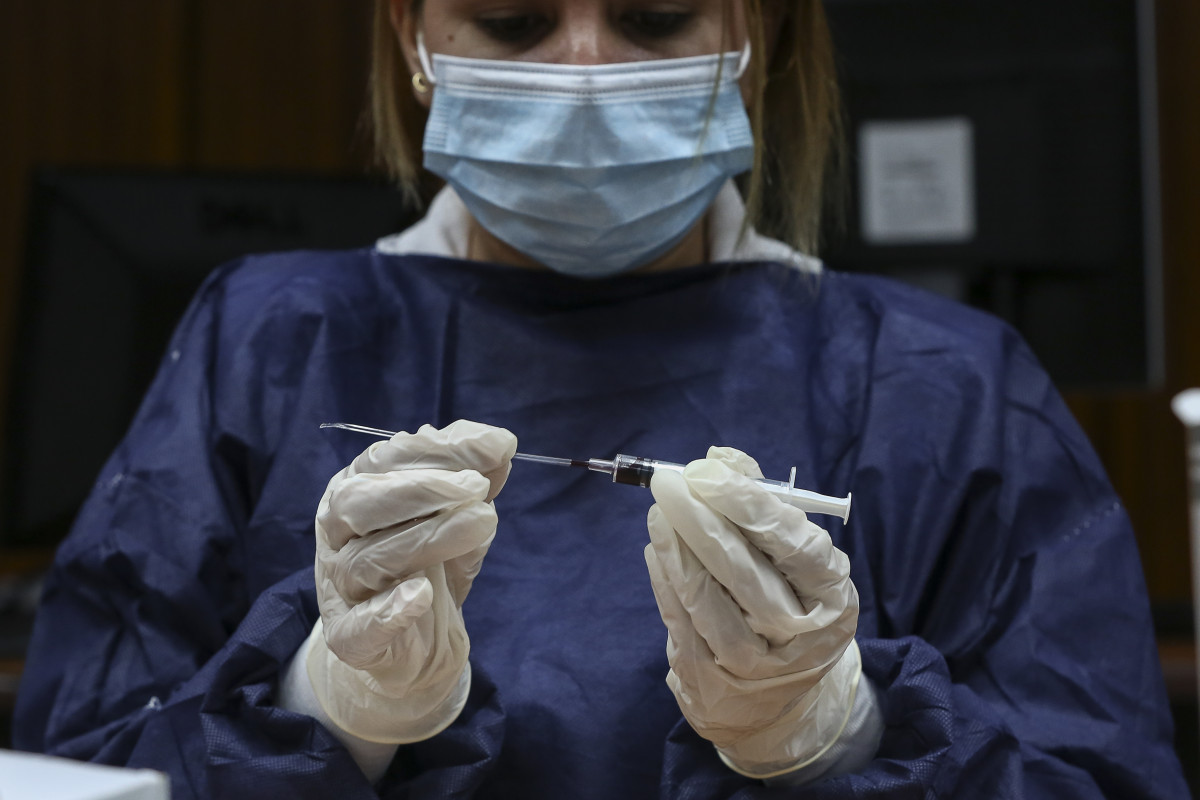
Moderna ha anunciado que la Junta de Monitoreo de Seguridad de Datos (DSMB, por sus siglas en inglés), independiente y designada por los Institutos Nacionales de Salud de Estados Unidos (NIH, por sus siglas en inglés), ha informado de que el estudio de fase 3 de ARNm-1273, su candidato a vacuna contra COVID-19, ha obtenido una eficacia de la vacuna del 94,5 por ciento en los primeros análisis.
Los resultados son las últimas noticias alentadoras que surgen del esfuerzo vertiginoso para desarrollar una vacuna contra el coronavirus y siguen un análisis provisional similar a principios de este mes de una colaboración entre Pfizer y la empresa alemana BioNTech , que sugiere que su vacuna es 90% efectiva para prevenir enfermedades. .
No se espera que la vacuna Moderna esté disponible fuera de los EE. UU. hasta el próximo año. La biotecnología dijo que tendría 20 millones de dosis listas para enviarse en los EE. UU. antes de finales de 2020 y esperaba fabricar de 500 millones a mil millones de dosis a nivel mundial el próximo año.
Moderna acordó acuerdos para proporcionar a los EE. UU. 100 millones de dosis, con la opción de comprar 400 millones más. Japón, Canadá, Suiza, Qatar e Israel también han firmado acuerdos, y la Comisión Europea tiene un "posible acuerdo de compra" de 8 a 160 millones de dosis. El Reino Unido decidió no participar en el plan de la UE, y Matt Hancock argumentó en julio que el gobierno podría obtener la vacuna más rápido por sí solo .

Escribe tu comentario