Descubren un metabolito intestinal clave en el origen de la aterosclerosis
El hallazgo, aún en fase preliminar, permite detectar alteraciones en el sistema vascular antes de que aparezcan los síntomas clínicos más graves,
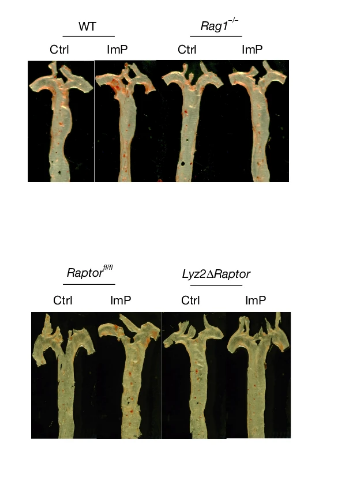
Una investigación innovadora liderada por el Centro Nacional de Investigaciones Cardiovasculares (CNIC) ha desvelado un hallazgo que podría cambiar radicalmente el diagnóstico y tratamiento de la aterosclerosis, la principal causa de muerte a nivel mundial. El estudio, publicado en la prestigiosa revista Nature, identifica el propionto de imidazol (ImP), un metabolito producido por la microbiota intestinal, como un factor causal y un nuevo biomarcador temprano de esta enfermedad.
Un marcador temprano y causal de la aterosclerosis activa
Las enfermedades cardiovasculares, que a menudo se originan por la aterosclerosis (el endurecimiento y estrechamiento de las arterias), siguen siendo la principal causa de mortalidad global. Aunque se controlan factores de riesgo clásicos como el colesterol alto, la hipertensión o el tabaquismo, la detección temprana es crucial. El equipo del CNIC, con el apoyo fundamental de la Fundación “la Caixa” (a través de su Convocatoria CaixaResearch de Investigación en Salud con casi un millón de euros), ha descubierto que el ImP se detecta en la sangre de personas con aterosclerosis activa incluso en etapas tempranas. Annalaura Mastrangelo, investigadora del CNIC y primera autora del estudio, explica que este metabolito "está producido exclusivamente por bacterias del intestino" y que "su presencia en sangre se relaciona con el desarrollo de aterosclerosis activa en personas aparentemente sanas".

La relevancia diagnóstica de este descubrimiento es inmensa. "Detectar este marcador en sangre representa una gran ventaja", subraya Mastrangelo, "dado que las pruebas actuales para identificar la aterosclerosis activa requieren técnicas de imagen avanzada, complejas y costosas, que a menudo no están cubiertas por la seguridad social. Los niveles de ImP en sangre ofrecen un marcador con valor diagnóstico para facilitar la identificación de personas sanas que tienen aterosclerosis activa y posibilitar su tratamiento temprano". Pero el ImP no es solo un marcador. Iñaki Robles-Vera, también primer autor del estudio, añade: "No solo observamos que el ImP está elevado en personas con aterosclerosis, sino que es un agente causal de la enfermedad." El consumo de ImP en modelos animales de aterosclerosis provocó la aparición de placas en las arterias. El mecanismo descubierto es que el ImP activa el receptor imidazolínico de tipo 1 (I1R), lo que genera un aumento de la inflamación sistémica que contribuye directamente al desarrollo de la aterosclerosis.
Una nueva vía para el tratamiento
Para David Sancho, jefe del laboratorio de Inmunobiología del CNIC y líder del estudio, "este descubrimiento es importante porque abre una nueva vía de tratamiento". La investigación publicada en Nature ha revelado que el uso de bloqueantes del receptor I1R previene la inducción de aterosclerosis por ImP y reduce la progresión de la enfermedad en modelos de ratón, incluso en aquellos inducidos por una dieta alta en colesterol. "Esto abre la posibilidad futura de un tratamiento combinado del bloqueo de I1R junto al bloqueo de la producción de colesterol para lograr un efecto que esperamos que sea sinérgico y que prevenga el desarrollo de aterosclerosis", asegura David Sancho. Estos hallazgos ofrecen "nuevas posibilidades para el diagnóstico precoz y el tratamiento personalizado y temprano de la aterosclerosis". En el futuro, además de los factores clásicos como el colesterol, la presencia de ImP en sangre podría ser un indicador clave de riesgo. Actualmente, el CNIC ya está trabajando en el desarrollo de fármacos que puedan bloquear los efectos perjudiciales de este metabolito.
Colaboración global para un avance traslacional
Aunque liderado por el CNIC, este estudio es fruto de una extensa colaboración global, tanto a nivel nacional como internacional. Han participado instituciones de renombre como el Mount Sinai Fuster Heart Hospital e Icahn School of Medicine at Mount Sinai en Nueva York (EEUU); el Instituto de Investigación Sanitaria Fundación Jiménez Díaz; la Universidad Autónoma de Madrid; el Centro de Investigación Biomédica en Red de Enfermedades Cardiovasculares (CIBER-CV); la Universidad de Gotemburgo (Suecia); la Universidad de Atenas (Grecia); Inmunotek S.L; la Universidad de Michigan (EEUU); el Hospital de La Princesa; el Centro de Metabolómica y Bioanálisis (CEMBIO) de la Universidad CEU San Pablo; la Universidad de Heidelberg (Alemania); y el Instituto de Investigaciones Biomédicas Sols-Morreale IIBM-CSIC. Este ambicioso proyecto ha recibido financiación de importantes entidades como el European Research Council, el Ministerio de Ciencia, Innovación y Universidades, la Agencia Estatal de Investigación, la Unión Europea a través de NextGeneration, y la ya mencionada Fundación “la Caixa”.

Escribe tu comentario